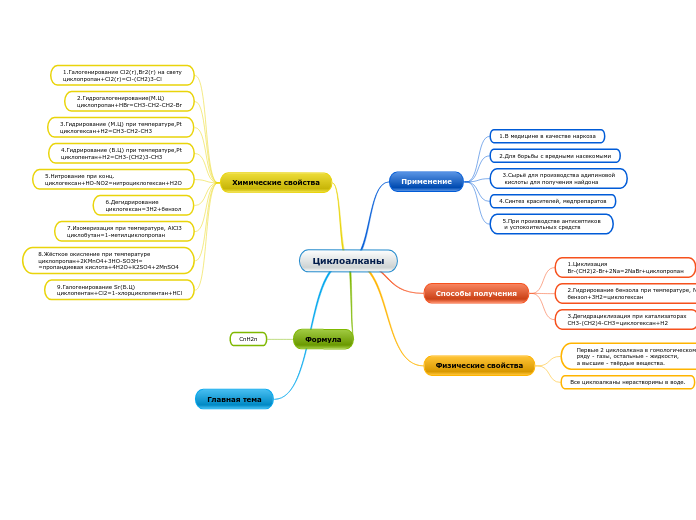
Циклоалканы
Применение
1.В медицине в качестве наркоза
2.Для борьбы с вредными насекомыми
3.Сырьё для производства адипиновой
кислоты для получения найдона
4.Синтез красителей, медпрепаратов
5.При производстве антисептиков
и успокоительных средств
Способы получения
1.Циклизация
Br-(CH2)2-Br+2Na=2NaBr+циклопропан
2.Гидрирование бензола при температуре, Ni
бензол+3Н2=циклогексан
3.Дегидрациклизация при катализаторах
CH3-(CH2)4-CH3=циклогексан+Н2
Физические свойства
Первые 2 циклоалкана в гомологическом
ряду - газы, остальные - жидкости,
а высшие - твёрдые вещества.
Все циклоалканы нерастворимы в воде.
Химические свойства
1.Галогенирование Cl2(г),Br2(г) на свету
циклопропан+Cl2(г)=Cl-(CH2)3-Cl
2.Гидрогалогенирование(М.Ц)
циклопропан+HBr=CH3-CH2-CH2-Br
3.Гидрирование (М.Ц) при температуре,Pt
циклогексан+Н2=CH3-CH2-CH3
4.Гидрирование (Б.Ц) при температуре,Pt
циклопентан+Н2=CH3-(CH2)3-CH3
5.Нитрование при конц.
циклогексан+HO-NO2=нитроциклогексан+H2O
6.Дегидрирование
циклогексан=3Н2+бензол
7.Изомеризация при температуре, AlCl3
циклобутан=1-метилциклопропан
8.Жёсткое окисление при температуре
циклопропан+2KMnO4+3HO-SO3H=
=пропандиевая кислота+4H2O+K2SO4+2MnSO4
9.Галогенирование Sr(Б.Ц)
циклопентан+Cl2=1-хлорциклопентан+HCl
Формула
CnH2n