Estructura atómica y tipos de enlace químico
Tipos de enlace químico
Enlace primario
Metálico
Se da entre átomos metálicos de un mismo elemento
los átomos ceden sus electrones de valencia para formar un mar de electrones.
Características
Buenos conductores de electricidad
Poseen alta ductilidad

Buenos conductores de calor
Covalente
Ocurre entre 2 o más NO metales
Se forman por medio de la compartición de electrones de valencia entre dos o más átomos.
Características
Resistencia
Dureza

Diamante (C)
Altos puntos de fusión
Iónico
Se da entre metal+no metal
Un átomo puede donar sus electrones de valencia a un átomo distinto, llenando la capa externa del segundo átomo.
Características
Sólidos a temperatura ambiente
Estructura cristalina

Sal de mesa NaCl
Solubles en agua y disoluciones acuosas
Enlace secundario
Van Der Waals
Las moléculas polares tienen un dipolo permanente como si fueran imanes con un polo positivo (δ+) y otro negativo (δ-). Así, la región positiva de la molécula atraerá la región negativa de otras moléculas cercanas y viceversa.
Tipos de enlaces Van Der Waals
Dipolo-dipolo inducido
Dipolo-dipolo
Propiedades
Aumento de los puntos de fusión y ebullición de un compuesto
Viscosidad

Agua H2O
Tensión superficial
Adhesión
Fuerzas de London
Ión-Dipolo
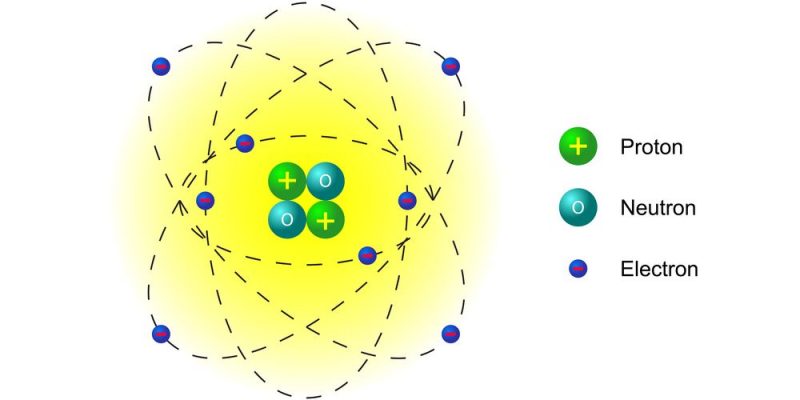
Estructura atómica
El átomo está formado por
Núcleo
Protones
Partículas subatómicas con carga positiva
Poseen una carga positiva de 1.6x10^-19 Coulombs
Neutrones
Partículas subatómicas con carga neutra
Electrones
Orbitan el núcleo del átomo y tienen carga negativa
Posee una carga negativa de 1.6x10^-19 Coulombs
Características del átomo
Número atómico
Número de protones en cada átomo
Masa atómica
Masa total del número promedio de protones y neutrones en el átomo en unidades de masa atómica
El número de Avogadro NA=6.022 x10^23 átomos/mol es el número de átomos o moléculas en un mol
Sus unidades son gramos/mol
Modelo atómico de Rutherford